初診はお電話でのご予約のみ
044-455-7500初診はお電話でのご予約のみ
044-455-7500肥満はうつと関連しやすく、また抗うつ薬による治療が体重増加に関連することがあります1)。
SerrettiとMandelliは2010年に短期的な抗うつ薬の治療ではアミトリプチリン(トリプタノール)、ミルタザピン(リフレックス・レメロン)、パロキセチン(パキシル)が体重増加に関連することを報告していました2)。
その後、ArterburnやGafoorらによって長期的な抗うつ薬の使用による体重変化の解析が行われ、抗うつ薬の内服継続2年目から3年目に最も体重が増加することがわかりました3)、(図1)。
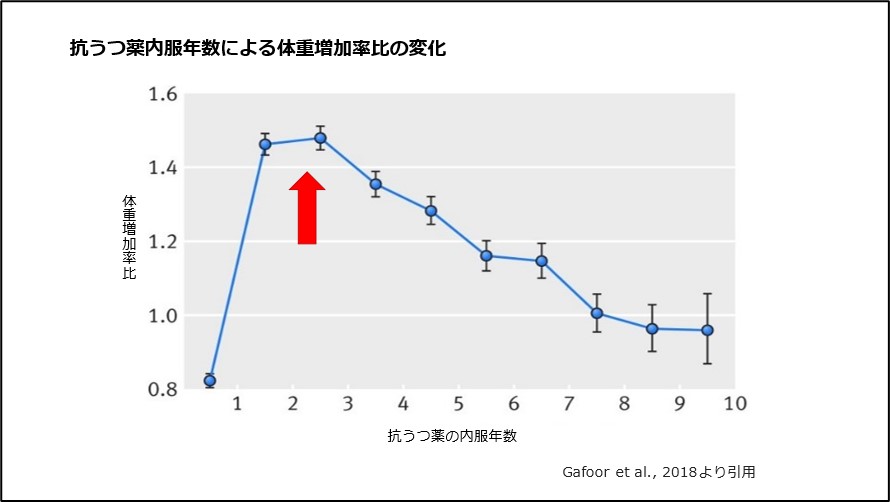
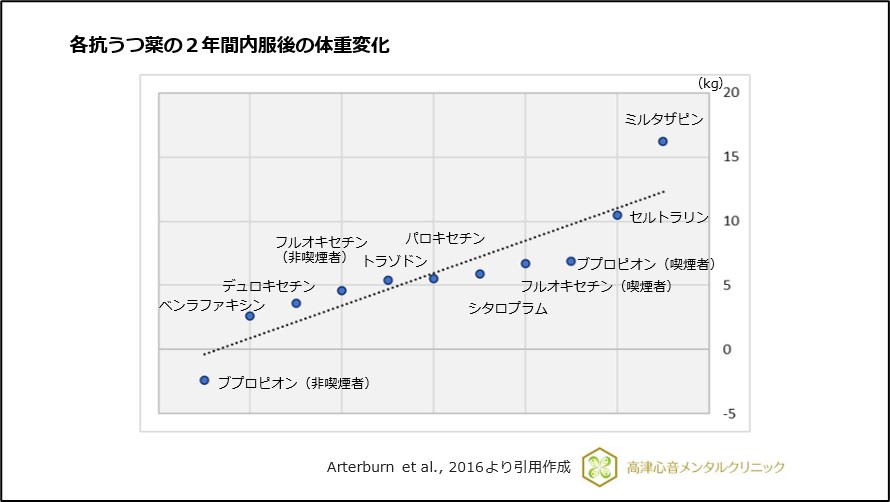
2年目時点の内服ではミルタザピン(リフレックス・レメロン)、セルトラリン(ジェイゾロフト)の体重増加割合が高く、SNRIのデュロキセチン(サインバルタ)、ベンラファキシン(イフェクサー)の体重増加割合が低い割合でした。
日本未承認のNDRI(ノルアドレナリン・ドパミン再取り込み阻害剤)のブプロピオンは体重が減少する結果でした4)、(図2)。
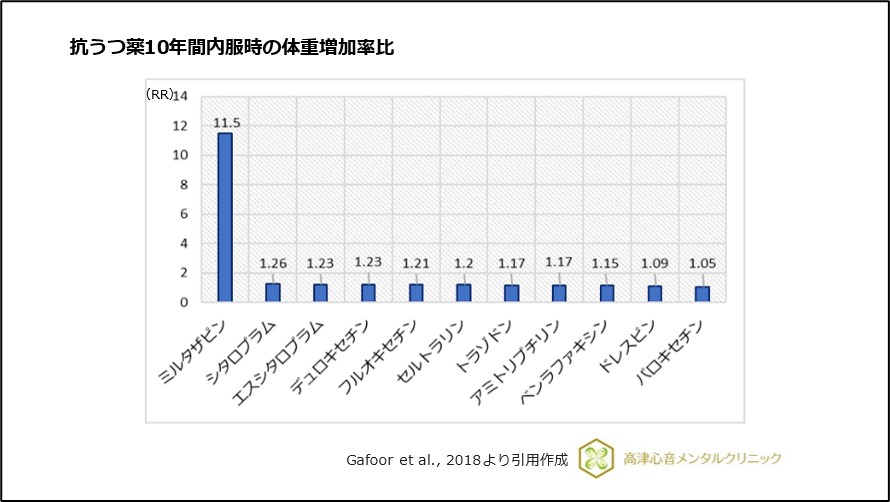
10年間の長期的追跡結果では体重増加の薬剤クラス別の体重増加率比は、NaSSA(ミルタザピン)>SSRI>SNRI>TCA(三環系抗うつ薬)の結果でした。
各抗うつ薬ではミルタザピンが体重増加に大きく関連し、その他の薬剤の差は小さいものでした2)、(図3)。
これらの結果からミルタザピンについては短期的結果と同様であるものの、パロキセチン(パキシル)の長期内服は一般にイメージされているものと違い、他の薬剤と比較し体重増加のリスクは高いとはいえないことがわかります。
ミルタザピンの体重増加はヒスタミンH1受容体阻害、セロトニン5-HT2C受容体阻害作用に加え、近年では視床下部のAMPK(AMP-activated protein kinase:AMP活性化プロテインキナーゼ)の活性化の関与が指摘されています5)。
視床下部AMPKの活性化は食欲の増加とともに脂肪組織での熱産生を減少させ、エネルギー代謝を低下させることがわかっています6)。
α-リポ酸の併用はミルタザピンの体重増加の抑制に有用である可能性が示唆されています7)。
SSRIの体重増加のメカニズムは短期と長期の2相性であることが報告されています。
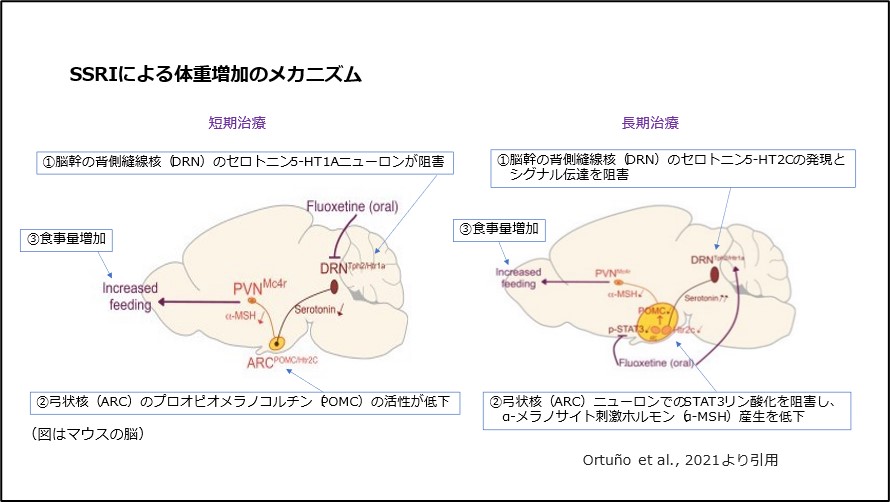
短期的には脳幹の背側縫線核(DRN)のセロトニン5-HT1Aニューロンが阻害され、満腹感を満たす弓状核(ARC)のプロオピオメラノコルチン(POMC)の活性が低下することが摂食行動につながります。
長期的には脳幹の背側縫線核(DRN)のセロトニン5-HT2Cの発現とシグナル伝達を阻害し、弓状核(ARC)ニューロンでのSTAT3リン酸化を阻害し、α-メラノサイト刺激ホルモン(α-MSH)産生を低下させることにより摂食行動を増加させます。(α-メラノサイト刺激ホルモンは食欲抑制に関与しています。)8)、(図4)。
抗うつ薬の体重増加では、図2からもわかるように喫煙しているかどうかや、普段の食事習慣、年齢等が抗うつ薬の内服とは別個に大きく関連します。
そのため、単に抗うつ薬を内服しているから体重が増加する、増加したとは言えず、必要な治療を優先しつつ、冷静な受け止めが必要と言えます。
うつ症状がある場合は、我慢せず早めの心療内科・精神科への受診をおすすめします。
まずはかかりつけ内科等で相談するもの1つの方法です。

