特徴・作用
ゾニサミドはてんかん発作を抑制する効果とパーキンソン病症状を改善する効果を有する薬です。
住友ファーマ社により1974年に合成され、てんかん治療薬としてエクセグランの商品名で1989年から発売されました。
2000年にけいれん発作が生じたパーキンソン病患者さんがゾニサミドを内服したところ、けいれん発作の改善とともにパーキンソン症状の改善がみられ、パーキンソン病への効果が見出されました1)。
その後、2015年よりパーキンソン病治療薬として、トレリーフの商品名で発売されることになりました。
トレリーフは、2018年に「レビー小体型認知症に伴うパーキンソニズム」に対する保険承認が追加されました。
ゾニサミドは主として、電位依存性ナトリウムイオンチャネルを阻害することと、T型カルシウムチャネルを阻害することにより抗てんかん作用を発揮します2)、3)。
また、主として、モノアミン酸化酵素B(MAO-B)を阻害することと、T型カルシウムチャネルを阻害することにより、パーキンソン症状を改善します4)、(図1)。
図1 ゾニサミド(トレリーフ)のパーキンソン症状改善の作用機序
パーキンソン病に対しては振戦などの運動症状だけでなく、睡眠障害などの非運動症状への有効性も報告されています5)。
また、神経保護機能を有する可能性が示唆されています6)、7)。
パーキンソン症状の改善に有効であることから、薬剤性パーキンソニズムの治療に使用されることもあります。
また、抗精神病薬による遅発性ジスキネジアに対する有効性も報告されています8)、9)。
剤型
先発医薬品のエクセグランは100mg錠と散剤20%があります。
トレリーフは口腔内崩壊錠(OD錠)25mgと50mgがあります(図2)。
図2 ゾニサミド(先発医薬品:エクセグラン・トレリーフ)の剤型(錠剤)
効能・効果
エクセグラン
エクセグランの効能・効果は以下となっています。
部分てんかんおよび全般てんかんの下記発作型となっています。
部分発作
- 単純部分発作[焦点発作(ジャクソン型を含む)、自律神経発作、精神運動発作]
- 複雑部分発作[精神運動発作、焦点発作]
- 二次性全般化強直間代けいれん[強直間代発作(大発作)]
全般発作
- 強直間代発作[強直間代発作(全般けいれん発作、大発作)]
- 強直発作[全般けいれん発作]
- 非定型欠神発作[異型小発作]
混合発作[混合発作]
トレリーフ
トレリーフの効能・効果は以下となっています。
OD錠 25mg
- パーキンソン病 (レボドパ含有製剤に他の抗パーキンソン病薬を使用しても十分に効果が得られなかった場合)
- レビー小体型認知症に伴うパーキンソニズム (レボドパ含有製剤を使用してもパーキンソニズムが残存する場合)
OD錠 50mg
- パーキンソン病 (レボドパ含有製剤に他の抗パーキンソン病薬を使用しても十分に効果が得られなかった場合)
用法・用量
エクセグラン
エクセグランの用法・用量は以下となっています。
通常、成人は最初1日100~200mgを1~3回に分けて内服します。
以後1~2週ごとに増量して通常1日量200~400mgまで漸増し、1~3回に分けて内服します。
なお、最高1日量は600mgまでとします。
小児に対しては、通常、最初1日2~4mg/kgを1~3 回に分けて内服します。
以後1~2週ごとに増量して通常1日量4~8mg/kgまで漸増し、1~3回に分けて内服します。
なお、最高1日量は12mg/kgまでとします。
血中濃度は10~20μg/mLが有効とされています10)、11)。
トレリーフ
トレリーフの用法・用量は以下となっています。
OD錠 25mg
本剤は、レボドパ含有製剤と併用します。
パーキンソン病では通常、成人で1日1回25mgを内服します。
なお、パーキンソン病における症状の日内変動(wearing-off 現象)の改善には、1日1回50mgを内服します。
レビー小体型認知症に伴うパーキンソニズムでは通常、成人で1日1回25mgを内服します。
OD錠 50mg
本剤は、レボドパ含有製剤と併用します。
通常、成人で1日1回25mgを内服します。
なお、パーキンソン病における症状の日内変動(wearing-off 現象)の改善には、1日1回50mgを内服します。
薬物動態
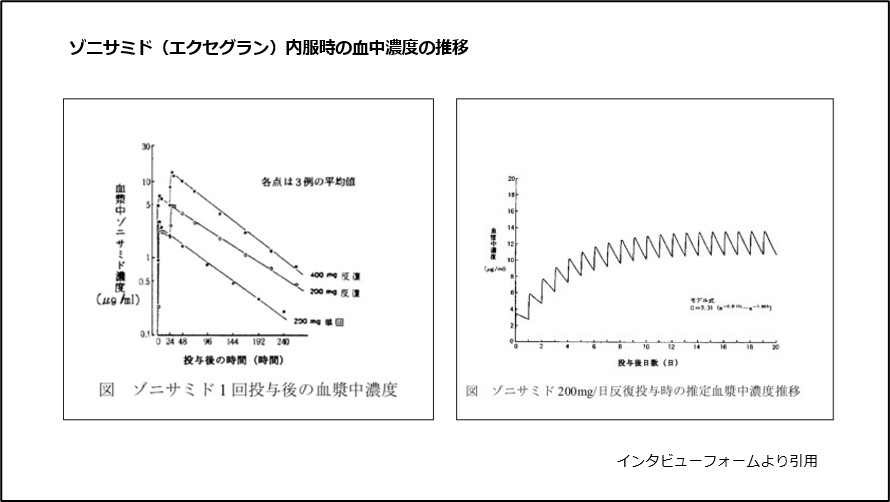
エクセグラン200mgを1回内服した際の血中濃度は約5.3時間後に最高濃度に達し、約63時間後に半減します。
毎日内服すると14~17日で一定の濃度に維持すると推定されています(図3)。
図3 ゾニサミド(エクセグラン)内服時の血中濃度の推移
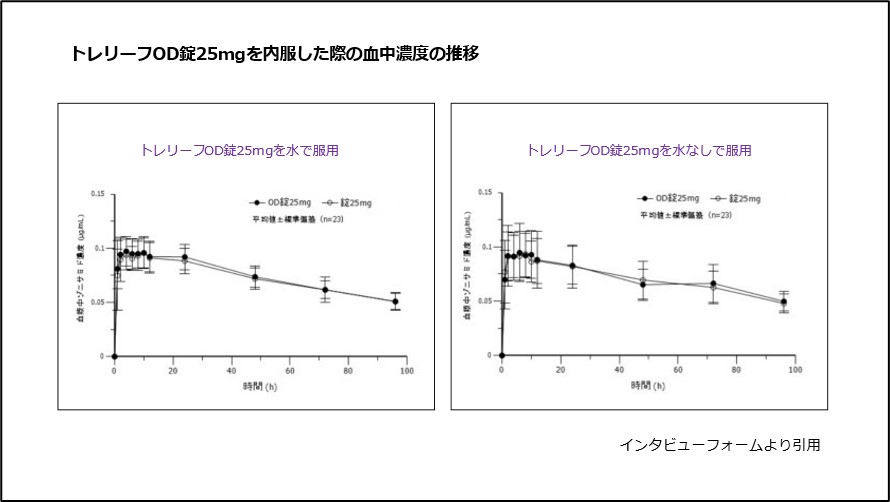
トレリーフOD錠25mgを水で服用した際は血中濃度は約8時間後に最高濃度に達し、約96.6時間後に半減します。
水なしで服用した際は血中濃度は約6時間後に最高濃度に達し、約119.1時間後に半減します(図4)。
図4 トレリーフOD錠25mgを内服した際の血中濃度の推移
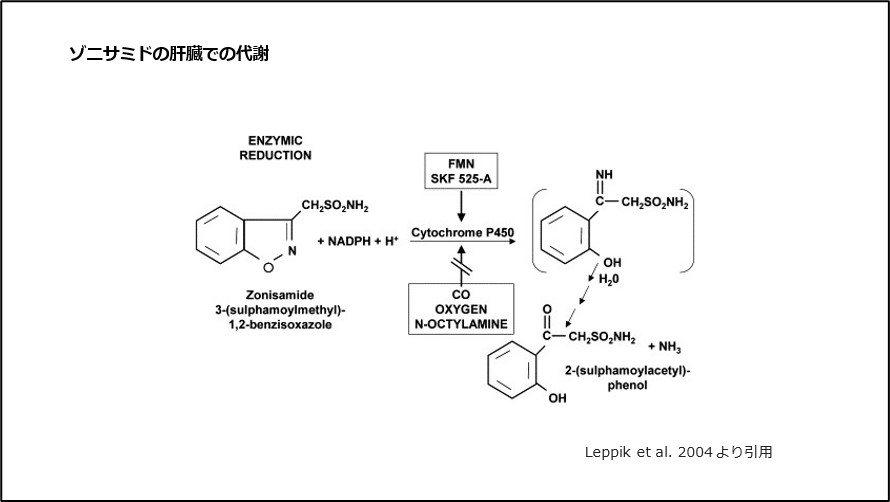
ゾニサミドは肝臓でアセチル化を受けてN-アセチルゾニサミドを形成し、CYP3A4により2-スルファモイルアセチルフェノールに代謝されます3)、(図5)。
図5 ゾニサミドの肝臓での代謝
副作用
エクセグランの重要な基本的注意に以下が挙げられています。
- 連用中における投与量の急激な減量ないし投与の中止により、てんかん重積状態があらわれることがあるので、投与を中止する場合には、徐々に減量するなど慎重に行うこと。
- 連用中は定期的に肝・腎機能、血液検査を行うことが望ましい。
- 眠気、注意力・集中力・反射運動能力等の低下が起こることがあるので、本剤投与中の患者には自動車の運転など危険を伴う機械の操作に従事させないよう注意すること。
- 用量調整をより適切に行うためには本剤の血中濃度測定を行うことが望ましい。
- 発汗減少があらわれることがあり、特に夏季に体温が上昇することがあるので、本剤投与中は体温上昇に留意し、このような場合には高温環境下をできるだけ避け、減量又は中止など適切な処置を行うこと。
- 投与中又は投与中止後に、自殺企図があらわれることがあるので、患者の状態及び病態の変化を注意深く観察すること。
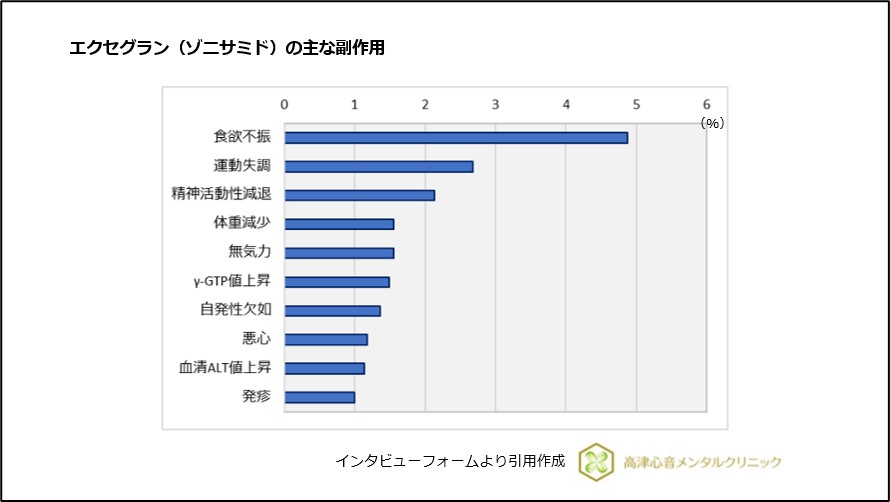
エクセグランは、承認時まで及び市販後調査の合計6,376例中1,575例(24.7%)に副作用発現を認め、主なものは以下でした(図6)。
- 食欲不振(4.88%)
- 運動失調(2.68%)
- 精神活動性減退(2.13%)
- 体重減少(1.55%)
- 無気力(1.55%)
- γ-GTP値上昇(1.49%)
- 自発性欠如(1.36%)
- 悪心(1.18%)
- 血清ALT値上昇(1.14%)
- 発疹(1.0%)
図6 エクセグラン(ゾニサミド)の主な副作用
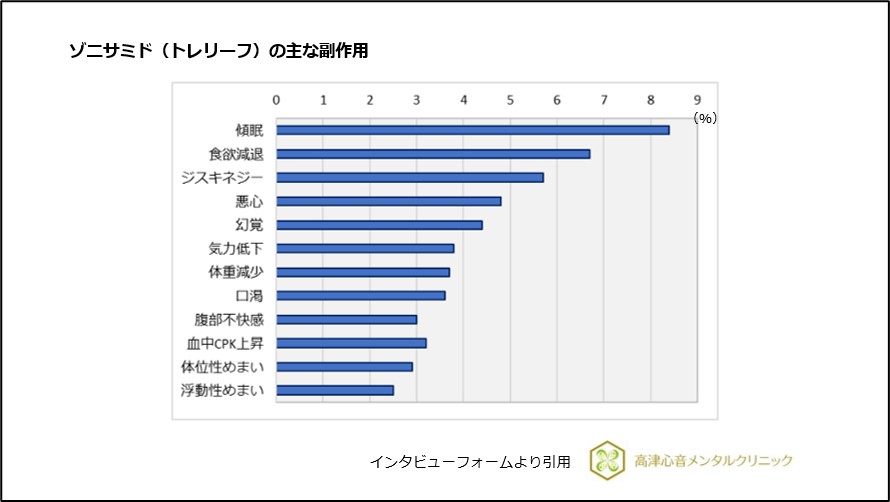
トレリーフは、国内臨床試験において842例中393例(46.7%)に副作用発現を認め、主なものは以下でした(図7)。
- 傾眠(8.4%)
- 食欲減退(6.7%)
- ジスキネジー(5.7%)
- 悪心(4.8%)
- 幻覚(4.4%)
- 気力低下(3.8%)
- 体重減少(3.7%)
- 口渇(3.6%)
- 腹部不快感(3.0%)
- 血中CPK上昇(3.2%)
- 体位性めまい(2.9%)
- 浮動性めまい(2.5%)
図7 ゾニサミド(トレリーフ)の主な副作用
有効性と安全性の解析では、パーキンソン病当事者ではでは眠気が生じる可能性が増えること、レビー小体型認知症当事者では打撲傷、食欲低下が生じる可能性が増えることが報告されています12)。
参考
- 1) Murata M, et al. : Zonisamide has beneficial effects on Parkinson’s disease patients. Neurosci Res, 397-9, 2001.
- 2) Biton V. : Clinical pharmacology and mechanism of action of zonisamide. Clin Neuropharmacol, 230-40, 2007
- 3) Leppik IE. : Zonisamide: chemistry, mechanism of action, and pharmacokinetics. Seizure, S5-9, 2004.
- 4) Li C, et al. : Zonisamide for the Treatment of Parkinson Disease: A Current Update. Front Neurosci, 14 : 574652, 2020.
- 5) Suzuki K, et al. : Zonisamide effects on sleep problems and depressive symptoms in Parkinson’s disease. Brain Behav, 11 : e02026, 2011.
- 6) Tsujii S, et al. : ,Zonisamide suppresses endoplasmic reticulum stress-induced neuronal cell damage in vitro and in vivo. Eur J Pharmacol, 746 : 301-7, 2015.
- 7) Arawaka S, et al. : Zonisamide attenuates α-synuclein neurotoxicity by an aggregation-independent mechanism in a rat model of familial Parkinson’s disease. PLoS One, 9 : e89076, 2014.
- 8) Caroff SN, et al. : Pharmacological treatment of tardive dyskinesia: recent developments. Expert Rev Neurother, 17 : 871-881, 2017.
- 9) Lerner PP, et al. : Tardive dyskinesia (syndrome): Current concept and modern approaches to its management. Psychiatry Clin Neurosci, 69 : 321-34, 2015.
- 10) Sobieszek G, et al. : Zonisamide: a new antiepileptic drug. Pol J Pharmacol, 55 : 683-9, 2003.
- 11) Peters DH, Sorkin EM. : Zonisamide. A review of its pharmacodynamic and pharmacokinetic properties, and therapeutic potential in epilepsy. Drugs, 760-87, 1993.
- 12) Kong L, et al. : Zonisamide’s Efficacy and Safety on Parkinson’s Disease and Dementia with Lewy Bodies: A Meta-Analysis and Systematic Review. Biomed Res Int, 2022 : 4817488, 2022.